- Contact Us
-

Tel:
+86-571-86879123 -

Fax:
+86-571-86910580
Home > PRODUCT CENTER > Medical Instruments
GUYOUDAO

Chemical Name
Bone Repairing Material
Specification
1mg/bottle,2mg/bottle
The only bone repairing material containing quantitative bioactivator rhBMP-2 in china.
A new generation of gene engineering bone repairing material.
Indication: BMP-2 is an osteoinductive bone repair material, indicated in filling and repairing for various reasons caused bone defect, bone non-union, delayed bone healing or un-healing, as well as treated in spinal fusion, joint fusion and orthopedic bone graft repair.
【产品名称】通用名:骨修复材料
【产品规格】1mgrhBMP-2/瓶;2mgrhBMP-2/瓶
【主要成分】为重组人骨形态发生蛋白质-2(rhBMP-2)和载体材料(羟基磷灰石、卵磷脂及药用明胶)组成。rhBMP-2是一种骨诱导生成因子,能诱导体内间充质干细胞定向分化为成骨细胞。
【结构特征】以重组人骨形态发生蛋白质-2(rhBMP-2)为原料,以药用明胶、大豆卵磷脂及羟基磷灰石为载体材料复合而成,它能诱导和促进骨和软骨的生成,因此可用于各种骨缺损及难愈合性骨折的修复治疗。
【作用机理】通过填充骨组织缺损、发挥骨诱导作用,达到组织修复,并在体内可被降解吸收。
【应用范围】该产品作为一种具有骨诱导生物活性的骨修复材料,可用于各种原因所致骨缺损、骨不连、骨延迟愈合或不愈合的填充修复,以及脊柱融合、关节融合及矫形植骨修复。
【物理性能】为多孔的白色或淡黄色海绵状固体材料。
【生物学性能】具有诱导成骨能力;生物相容性好;能在体内降解吸收。
【使用方法】本产品必须由具有专业知识的骨外科医生根据病人的具体情况及创伤、缺损部位体积大小确定植入剂量,单一部位建议使用剂量为4-6mgrhBMP-2,一次性使用最大剂量为6mgrhBMP-2。本产品可单独使用,也可与常规治疗方法配合使用。如缺损部位较大,可与自体骨/同种异体骨或其他可降解植骨材料联合使用。
【注意事项】
1、本产品无力学强度,使用在受力部位仍须进行机械固定。
2、本产品使用在关节部位,应尽量避免放置到关节腔内。
3、一次性使用本产品剂量不要超过6mgrhBMP-2。
4、本产品是多孔性的海绵状固体,在植入时可以进行适当挤压,也可以根据病人手术部位需要的大小或形状,在手术台上用手术剪进行小范围修整。
5、本产品在填充植入前应先将植入部位止血,植入后应避免冲洗伤口,并缝合软组织、以免活性成分流失,应避免引流。
6、对于治疗骨不连或陈旧性骨折,应打通两端的骨髓腔,以使rhBMP-2能与靶细胞直接接触。
7、植入后如出现积液或轻度炎症反应,仅需做对症处理和抗感染,如这些反应持续时间较长,并有加重趋势,必须去除植入物并清创。
8、患者使用本产品后若出现过敏,轻者应及时给予对症治疗,重者必须去除植入物。
9、本产品为灭菌产品,若包装开封或破损不得使用,防止造成不良反应。
10、在使用过程中,不得与其他化学物质(如酸、碱等化学物质)混合使用。以防止化学物质改变产品的性能。
【禁忌症】
1、有严重心、肾功能不全、肝功能损害及造血功能障碍者禁用。
2、有严重肿瘤史者禁用。
3、需要全身联合应用糖皮质激素者慎用。
4、代谢性骨病患者慎用。
5、妊娠、哺乳期妇女、儿童慎用。
【副作用】有少数患者会有低热、创口渗出、肿胀等反应,会自然消退或对症治疗后消退。
【并发症】本产品在临床试验中,尚未发现并发症。
【储存条件】储存于2-8℃,避免有害辐射。
【有效期】本产品通过Co60辐射达到无菌要求,有效期为两年。具体日期见外包装盒。请在标注的有效日期之前使用。
【产品注册号】国食药监械(准)字2014第3460233号
【执行标准】注册产品标准YZB/国7793-2013
【生产企业】杭州九源基因工程有限公司
【生产企业许可证编号】浙食药监械生产许20110097号
【注册地址】杭州经济技术开发区八号大街东
【生产地址、邮编】杭州市莫干山路866号(石祥路700号)310011
【售后服务单位】杭州九源基因工程有限公司
【联系电话】0571-86910099总机转
创伤修复
病例1:胫骨骨折
患者:男,57 岁,外伤致右膝肿痛伴活动受限,因疼痛拒动,较对侧明显肿胀,增粗约2cm,右胫腓骨X 线右胫骨近端骨折,右腓骨近端、中下段骨折,行胫骨骨折切开复位骨优导®2mg 植骨修复内固定术。
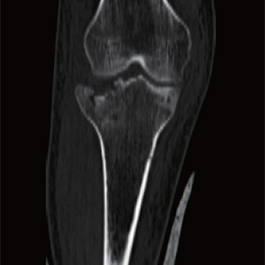
术前CT片示:胫骨平台劈裂塌陷。
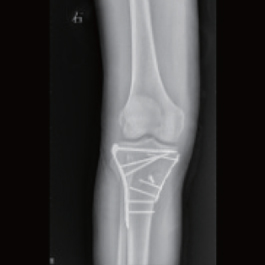
术后1周x线片示:骨折断端对位对线良好,骨折线可见。
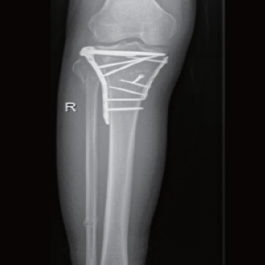
术后6月x线片示:骨折线模糊,内固定完好。
病例2:胫骨骨折
患者:男,71 岁,车祸致左膝疼痛,活动受限,拍X 片示左胫骨平台骨折,行切开复位骨优导®2mg 植骨修复内固定术,术后随访18月骨折修复。
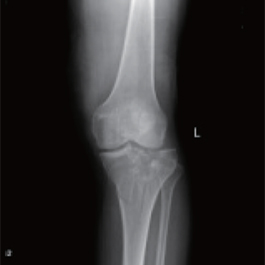
术前X线片示:有骨质破坏,平台劈裂塌陷。

术后1周X线示:骨折对位对线良好,骨折线清晰清晰可见。
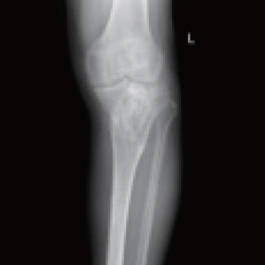
术后18月X线示:骨折完全修复,内固定拆除。
病例3: 跟骨骨折
患者:男,38,外伤致右足跟部肿胀,压痛伴活动受限,摄X 片示右跟骨骨折,行右跟骨骨折切开复位骨优导®2mg 植骨内固定术,术后15 月骨折修复,内固定拆除。
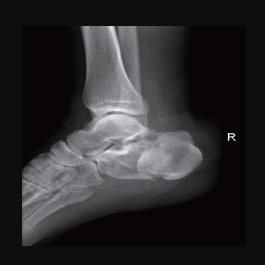
术前X线片示:跟骨骨折,骨折错位。
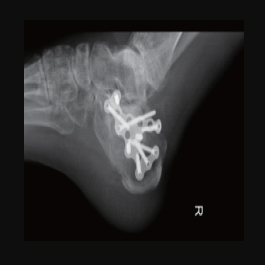
术后4月X线片示:骨折线模糊,内固定完好。
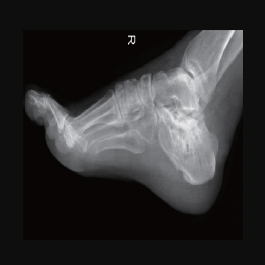
术后15月X线片示:骨折完全修复,内固定拆除。
病例4:腕骨及尺骨骨折
患者:女,57 岁,外伤致左腕肿胀、疼痛,畸形明显, 左腕关节活动受限较健侧肿胀,增粗约2cm,X 线片示左侧腕骨及尺骨远端粉碎性骨折,周围软组织肿胀,行切开复位骨优导®2mg 植骨内固定术。
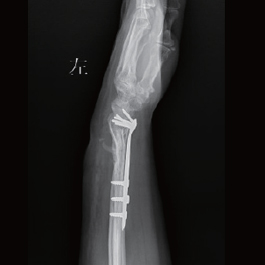
术后1周X线片示:骨折对位对线,骨折线清晰可见,钢板内固定。
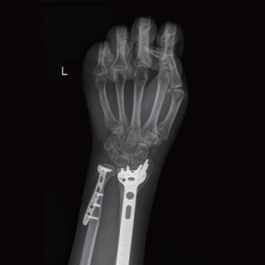
术后12月X线片示:骨折线模糊,内固定位置完好。
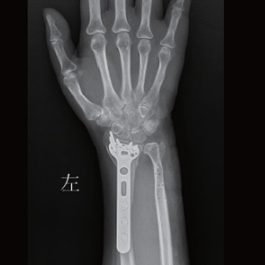
术后14月X线片示:尺骨骨折修复,内固定拆除,桡骨骨折线模糊,内固定完好。
病例5: 胫骨骨不连
患者:男性,外伤致胫骨骨折,手术治疗,2012 年10 月29 号X 线提示胫骨骨折未愈合、胫骨骨不连,再次手术骨优导®2mg植骨修复外固定改为钢板内固定,术后16月骨折修复,行钢板拆除术。
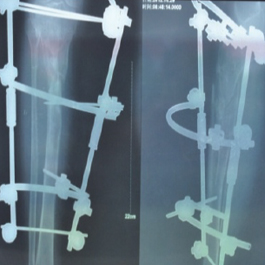
术前X线片示:骨折外固定术后骨折线清晰可见,骨不愈合。
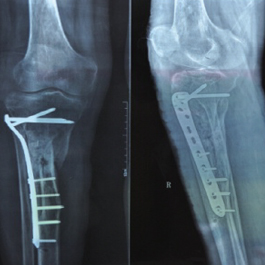
术后2周X线片示:骨折对位对线,内固定位置完好。
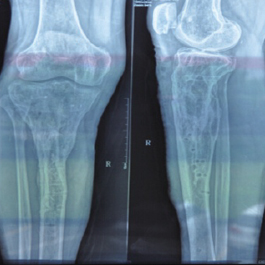
术后16月X线片示:骨折完全修复,内固定拆除。
病例6:肱骨骨不连
患者:女,32 岁,左肱骨不连18 年, 2012年4 月再次手术植入骨优导®2mg,术后18月骨折修复良好。
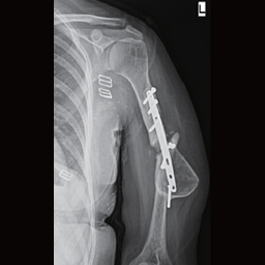
2013年3月20X线片示:折断端硬化,内固定物失效。
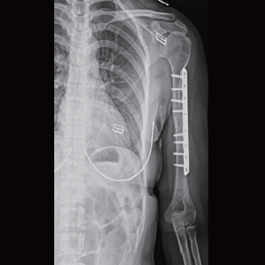
术后8月X片示:骨折端模糊,内固定完好。
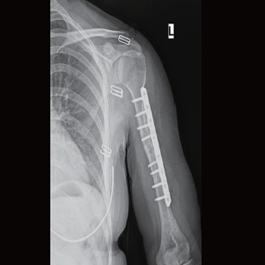
术后18月X片示:骨折修复良好。
病例7:尺骨骨不连
患者:男,35 岁,2 年前左前臂尺骨骨折,行切开骨折端自体骨植骨钢板内固定术治疗,术后1 年复查X 线片示骨折不愈合,断端骨硬化。再次手术予行切开疤痕切除,骨折断端自体骨骨优导®2mg 植骨,术后6 月复查显示骨折愈合良好。
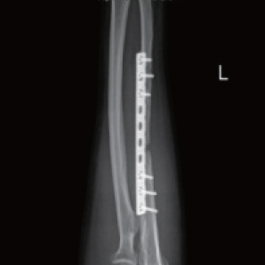
术前X线片示:尺骨骨折术后骨折不愈合,断端骨硬化 。
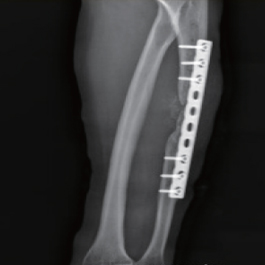
术后1周X线片示:骨折断端植入骨优导®2mg+自体骨。
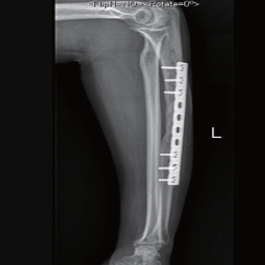
术后6月X线片示:骨折端有大量新骨形成,骨折线模糊,内固定完好,愈合良好。
病例8:股骨颈骨不连
患者,女,20 岁外伤致股骨颈骨折,内固定术后8 月余内固定物断裂,股骨颈骨不愈合,再次手术骨折端植入骨优导®2mg 钢板内固定,术后15 月骨折修复,内固定物拆除。
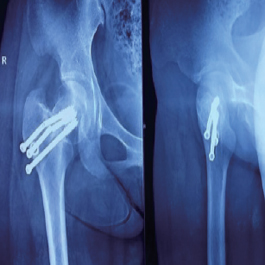
2013年8月X片示:内固定物断裂 ,骨折线清晰可见。
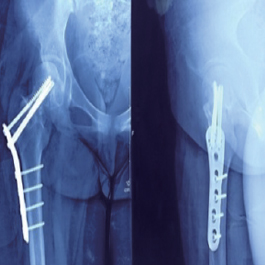
2013年11月X片示:再次手术,钢板内固定,骨折对位对线。
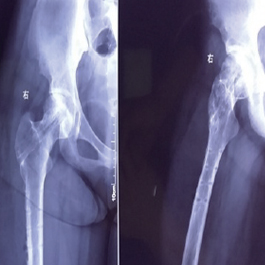
术后15月X片示:骨折修复,内固定拆除。
脊柱修复
病例1:腰椎椎间融合
患者:男性, 42 岁,右侧腰腿痛1 年,向右下肢小腿放射至右足外侧,劳累时加重, 平卧休息后缓解,无夜间疼痛加重,诊断为:“腰椎管狭窄并腰椎间盘突出症”,查体:脊柱腰段生理弯曲变直,无明显侧凸畸形,椎旁肌肉紧张痉挛,有压痛,腰椎后伸或侧屈时可诱发疼痛,前屈时症状缓解,右侧拇趾及足背伸力稍减弱。行腰椎后路滑脱复位L3/4、L4/5 椎管扩大减压,椎间盘切除,每个节段骨优导®1mg+ 自体骨融合,椎弓根内固定术,术后患者腰腿痛症状消失。
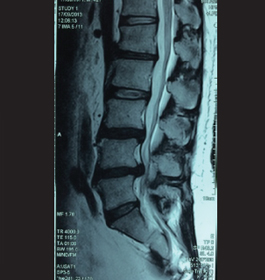
术前腰椎MRI: L3/4、L4/5椎间盘向后突出,双侧神经根受压,椎管狭窄, L 3、4椎体轻度向后滑脱,腰椎退行性变。
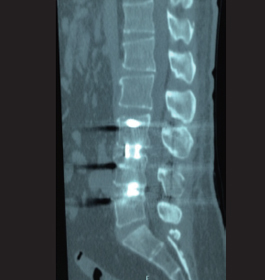
随访3月复查CT提示:L3/4、L4/5椎间已经有骨痂形成。
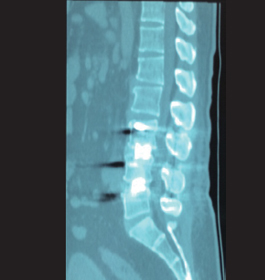
随访10月CT提示:L3/4、L4/5已经骨性融合,患者无腰痛等不适症状。
病例2:腰椎椎体骨折
患者: 男、67 岁,骑电动车时受到颠簸,当即觉腰背部疼痛,活动受限,腰1 棘突旁压痛叩痛明显,无双下肢放射痛,会阴部感觉正常,双下肢运动感觉正常,X线检查L1 压缩性骨折,胸腰椎退行性变,行腰椎后路切开复位L1 椎体骨优导®+ 自体骨植骨修复内固定术。

术前X线示:L1压缩性骨折,椎体退行性变。
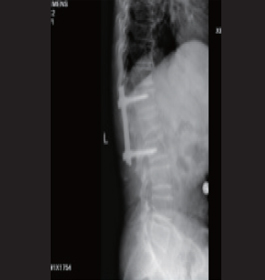
术后1周X线示:T1 和L2钉棒固定。
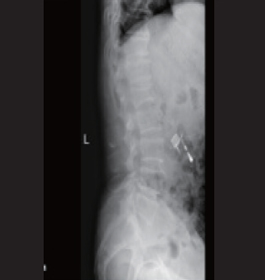
术后15个月X线示:骨折修复内固定拆除。
病例3:腰椎椎间融合
患者:女性, 52 岁,左侧腰腿痛1 周,疼痛向左大腿后直至小腿、足背放射,劳累时加重, 平卧休息后缓解,症状逐渐加重,今站立及直腰行走困难,无夜间疼痛加重,严重影响日常生活,诊断为腰椎管狭窄症,行L3/4、L4/5 椎管扩大减压,椎间盘切除,神经松解,每节段骨优导®1mg+ 自体骨植骨融合内固定术,术后症状消失出院,出院后未发生腰腿痛等不适症状,日常生活无影响。
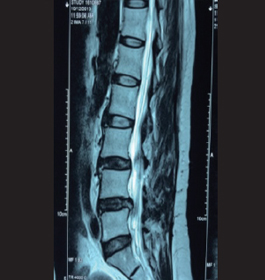
术前腰椎MRI:L3/4-L5/S1椎间盘变性,L3/4椎间盘膨出;L4/5椎间盘向左后方脱出,左侧神经根受压;L5/S1椎间盘向后突出; 腰椎退行性变。
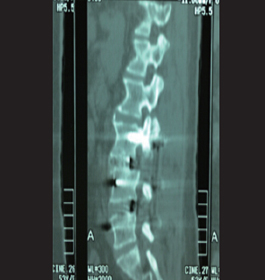
随访6月CT提示:L3/4、L4/5椎间骨痂形成。 随
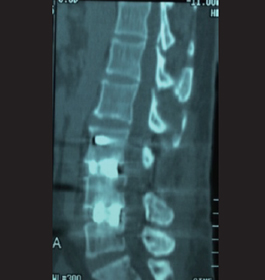
随访1年CT提示:L3/4、L4/5骨性融合,患者无腰痛等不适。
病例4 :颈椎椎间融合
患者:男性,37 岁双手麻木伴双下肢无力三年,双手尺侧三指麻木,握筷子较费力,并有双下肢小腿后方酸胀,伴行走及爬楼梯时费力,行走时有踩棉花样感觉, MRI C4-6,c6-7 椎间盘突出,压迫相应的硬膜囊和神经根,诊断为脊髓型颈椎病,行C4-5,C5-6 椎间融合术,每个节段融合器内植入骨优导®0.25mg 及自体骨赘。
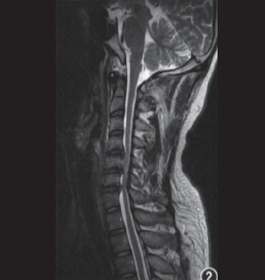
2013.4.3 MRI:C4-6,C6-7椎间盘突出,后纵韧带骨化,压迫相应硬膜囊和神经根。
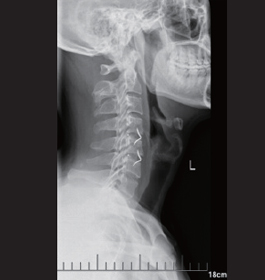
术后3个月X线片示:颈椎生理曲度改善,融合器与椎体界面有骨小梁通过。
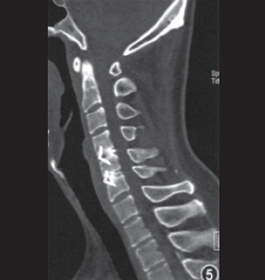
术后3个月CT提示:治疗节段到达骨性融合。
关节修复
病例1 : 股骨头坏死
患者:女22 岁, 双侧股骨头坏右侧B 型左侧C1型打压植骨术后5 年,CT 显示植骨生长良好,关节功能正常(Harris 评分 96),术后7 年关节维持正常,股骨头维持正常外形。
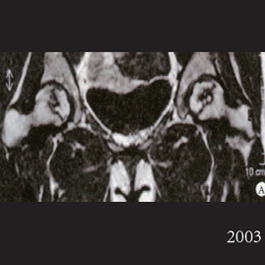
手术前
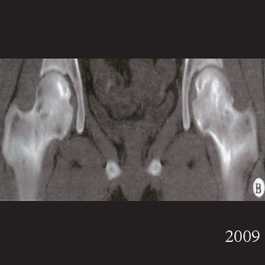
术后随访5年
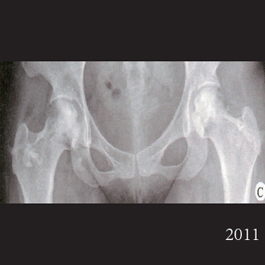
术后随访7年
病例2 : 股骨头坏死
患者:女31 岁, SARS 患者骨坏死
(1)MRI 双侧股骨头坏死, 右Ⅱb 型(B 型)左Ⅱc型(C1 型)
(2)打压植骨术( 未加BMP2)后坏死修复不完全,仍遗留股骨头软下病灶未完全修复,5 年随访关节功能优 ( Harris评分96 分)
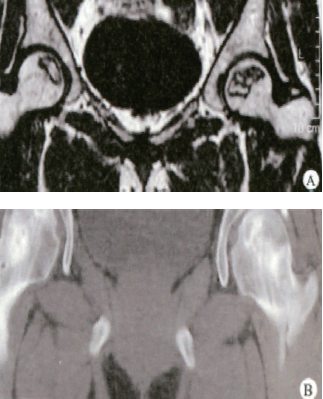
术后随访5年
病例3 :股骨头坏死
患者:女30 岁SARS 患者骨坏死
(1)MRI 双侧股骨头坏死 右Ⅱc 型C3 型左Ⅱb 期B 型打压植骨术(未加BMP2)
(2)5 年后CT 显示病灶修复好关节功能优
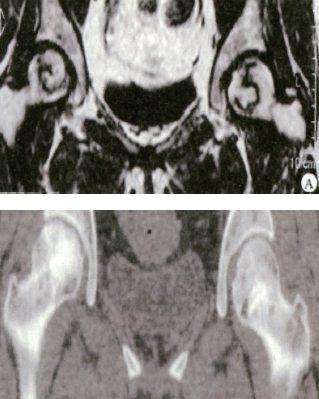
术后随访5年

Through ten years’ hard working, our company has developed “the only bone repairing material containing quantitative bioactivator rhBMP-2 in China”, namely, “Guyoudao”, which has proprietary intellectual property rights. The project was supported by Chinese 863 Program (Z18-03-28). The product was approved for marketing in the year 2009 by CFDA. Its registration No. is: CFDA device (approval) 2014 No.: 3460233.
Clinically, “Guyoudao” is indicated as a bone repair material for the treatment of bony defects, bone nonunion, bone delayed union or non-union, resulted from various causes, spinal fusion, joint fusion, and orthopaedic implantation. The product has good osteogenesis ability, biocompatibility and in vivo degradability. The product filled the gap of bone repairing material with bioactivity in China. Many a clinical data has proven that Guyoudao was clearly better than other bone repairing materials in spinal fusion, bone nonunion repairing. In the clinical study, several experts had articles published on the discussion and verification of the good efficacy of Guyoudao. Please refer to the annexed materials for the detailed information about the product